COVID-19 : le taux de létalité encore plus faible que ce qui était attendu
Publié le 06/03/2023 à 18h02 , mis à jour le 06/03/2023 à 18h02

Magali RégnierJournaliste
en collaboration avec Dr Gérald Kierzek (Directeur médical)
Trois ans après le début de la pandémie, une analyse menée sur 38 études nationales différentes nous apprend aujourd’hui que le Covid-19 est associé à un taux de létalité relativement faible. Et bien plus que ce que nous imaginions à son arrivée.
Sommaire
- Un taux de létalité très faible avant 60 ans
- « Une étude qui confirme ce qu’on voit sur le terrain »
Avons-nous surestimé la menace du Covid ? Probablement. L’idée n’est pas de relayer une théorie complotiste, mais d’exposer les résultats d’une vaste étude de l’université de Stanford, menée sur 38 pays 3 ans après le début de la pandémie.
Un taux de létalité très faible avant 60 ans
Des chercheurs américains et européens ont étudié le « Taux de létalité par infection, stratifié par âge du COVID-19 dans la population non âgée » avant l’introduction des vaccins COVID-19. Un taux qui s’est avéré après analyse aussi bas que 0,03% et 0,07% pour les personnes âgées de 0 à 59 ans et de 0 à 69 ans, respectivement, rapporte le document. Des estimations inférieures à ce que les calculs précédents avaient suggéré.
Autrement dit : 99,97 % des personnes de moins de 60 ans qui ont contracté le COVID-19 ont survécu. Ajoutez les personnes dans la soixantaine à la cohorte, et les taux de survie restent toujours solides à 99,93 %. En détail, selon les tranches d’âges, le taux de létalité est celui-ci :
- 0-19 ans : 0,0003 %
- 20-29 ans : 0,002 %
- 30-39 ans : 0,11 %
- 40-49 ans : 0,035 %
- 50-59 ans : 0,123 %
- 60-69 ans : 0,506 %
En moyenne, cela signifie que seuls cinq décès surviendraient parmi un millier de sexagénaires infectés. L’analyse actuelle souligne également que le taux de létalité est beaucoup plus faible dans les populations plus jeunes, que ce qui était précédemment suggéré. Elle affirme ainsi : « Ces chiffres de létalité covid sont légèrement plus élevés chez les 0-69 ans que les décès de la grippe saisonnière (sur les trois années avant covid). Ils restent cependant inférieurs à la grippe quand on prend uniquement les personnes de moins de 60 ans ».
Les chercheurs ont également constaté que les taux de létalité étaient plus élevés chez les hommes que chez les femmes, et que les personnes atteintes de certaines maladies sous-jacentes, comme le diabète, avaient un risque plus élevé de décès dû à une infection à COVID-19.
La différence entre taux de létalité et de mortalité Le taux de mortalité désigne le pourcentage de morts par rapport au nombre d’individus d’une population donnée dans une période donnée. Le taux de létalité ne se rapporte pas à toute une population mais seulement à une portion de celle-ci à savoir les personnes infectées et donc porteuses de la maladie en question. Il est donc plus précis pour donner le nombre de victimes.
« Une étude qui confirme ce qu’on voit sur le terrain »
Pour le Dr Kierzek, urgentiste et directeur médical de Doctissimo, cette large étude menée sur des millions de données ne fait que confirmer ce qui est observé sur le terrain.
“On voit bien que sur une tranche d’âge sans pathologie, chez les moins de 65 ans, quand on n’a pas de facteur de risque, la létalité est extrêmement faible. D’où le concept de « syndémie » pour qualifier le rôle du SARS-Cov2. Le Covid-19 est davantage un accélérateur de pathologie et/ou de grand âge qu’une menace en lui-même. Cela remet en perspective tout ce qu’on a pu dire ou penser pendant la crise, quand on parlait de taux très élevés de mortalité ».
Ces résultats soulignent l’importance de cibler les politiques de prévention en direction des groupes à risque, tels que les personnes âgées et les personnes atteintes de maladies sous-jacentes.
Sources
- Pezzullo AM, Axfors C, Contopoulos-Ioannidis DG, Apostolatos A, Ioannidis JPA. Age-stratified infection fatality rate of COVID-19 in the non-elderly population. Environ Res. 2023 Jan 1;216(Pt 3):114655. doi: 10.1016/j.envres.2022.114655. Epub 2022 Oct 28. PMID: 36341800; PMCID: PMC9613797.
Eur J Clin Invest. juin 2022 ; 52(6) : e13782.
Publié en ligne le 5 avril 2022. doi: 10.1111/eci.13782
La fin de la pandémie de COVID‐19
Jean PA Ioannidis 1
La fin de la pandémie de COVID‐19 – PMC.pdf
Abstract
Eur J Clin Invest. juin 2022 ; 52(6) : e13782.
Publié en ligne le 5 avril 2022. doi: 10.1111/eci.13782
PMCID : PMC9111437 PMID : 35342941
Il n’existe pas de définition quantitative largement acceptée de la fin d’une pandémie telle que celle de la COVID‐19. La fin de la pandémie due à un nouveau virus et la transition vers l’endémicité peuvent être définies sur la base du fait qu’une proportion élevée de la population mondiale possède une cer‐ taine immunité contre une infection naturelle ou une vaccination. D’autres considérations incluent la diminution du nombre de morts, la diminution de la pression sur les systèmes de santé, la réduction des risques personnels réels et perçus, la suppression des mesures restrictives et la diminution de l’attention du public. Un seuil de 70 % de la population mondiale ayant été vaccinée ou infectée a probablement déjà été atteint au cours du second semestre 2021. L’endémicité peut encore montrer des pics d’infec‐ tions et de saisonnalité importants, mais généralement une charge clinique moindre, même si certaines zones sont encore plus touchées. autres. Le nombre de décès et les chiffres d’occupation des soins in‐ tensifs concordent également avec une transition vers l’endémicité d’ici fin 2021/début 2022. Le risque personnel de la grande majorité de la population mondiale était déjà très faible fin 2021, mais le risque perçu pourrait encore être largement surestimé. Des mesures restrictives très strictes persistaient dans de nombreux pays début 2022. L’attention gargantuesque de la part des médias d’information, des réseaux sociaux et même des cercles scientifiques devrait être tempérée. Les responsables de la santé publique doivent déclarer la fin de la pandémie. Les conséquences à moyen et long termes des vagues épidémiques et des mesures adoptées sur la santé, la société, l’économie, la civilisation et la démocratie peuvent perpétuer un héritage pandémique longtemps après la fin de la pandémie elle-même…
1. INTRODUCTION
Prétendre à une date de fin horodatée pour la pandémie de COVID‐19 est précaire. Il n’existe pas de dé‐ finition rigoureusement quantitative des pandémies, encore moins de leur fin. 1 , 2 En termes de diction‐ naire, une pandémie est « une épidémie qui se produit à l’échelle mondiale ou sur une zone très vaste,
traversant les frontières internationales et affectant généralement un grand nombre de personnes ». 3 Pour éviter de qualifier de « pandémies » toutes les vagues virales saisonnières, une gravité inhabituelle (nombre de morts, charge des soins de santé) peut être recherchée. Cependant, tous les nouveaux virus qui se propagent à grande échelle n’ont pas un fardeau clinique élevé. Ainsi, on peut qualifier la large propagation d’un nouveau virus (contre lequel les populations ont peu d’immunité préalable) de pandé‐ mie, quelle que soit sa gravité. Il faut définir soigneusement la manière dont le terme « pandémie » est utilisé pour éviter les malentendus. Une fois qu’un seuil élevé d’immunité de la population (contre une infection ou une vaccination) est atteint, la pandémie passe à une phase endémique.
La sélection d’un seuil d’immunité quantitatif est arbitraire. Les seuils définis sur des considérations de base du nombre de reproduction (1−(1/R 0 )) font de nombreuses hypothèses, ne permettent pas correc‐ tement l’hétérogénéité de la population, dépendent d’estimations de R 0 qui peuvent ne pas être exactes et devraient changer lorsque des variantes avec des valeurs différentes R 0 émerge et devient dominant. En réalité, le seuil devrait être élevé, mais pas 100 %. Il est probable que des segments considérables de la population resteront non vaccinés malgré tous les efforts de campagne de vaccination, et certaines personnes non vaccinées pourraient encore échapper à l’infection pendant de nombreuses années. Pour les agents infectieux non éradiqués, la transmission communautaire se poursuit avec des vagues saison‐ nières récurrentes et des pics de différentes hauteurs au cours de la phase endémique et avec de grandes différences selon les pays et les lieux. Malgré des taux élevés de vaccination et d’infections antérieures, l’immunité peut s’avérer insuffisante pour protéger contre une infection bénigne et la transmission (en‐ core moins lorsque de nouveaux variants apparaissent), mais elle peut quand même diminuer considé‐ rablement les conséquences graves. (4)
Si la transition vers l’endémicité du SRAS-CoV-2 nécessite un seuil préalable de vaccination/infection de 70 %, ce seuil a probablement déjà été atteint à l’échelle mondiale en 2021, comme indiqué ci-des‐ sous. Cependant, plusieurs autres considérations doivent être évaluées avant de reléguer en toute sécuri‐ té la pandémie au passé. Ceux-ci incluent le nombre persistant de décès, le fardeau clinique, le risque personnel réel et perçu, les mesures continues prises contre le COVID‐19, l’attention du public et l’héri‐ tage des vagues épidémiques et des mesures adoptées.
2. IMMUNITÉ DES POPULATIONS
Fin 2021, 58 % de la population mondiale avait reçu un vaccin et 49 % avait été complètement vaccinée 5 (même si le terme « entièrement » peut être un terme impropre à long terme). La proportion de per‐ sonnes infectées est incertaine, car seule une minorité d’infections est documentée par des tests. 6 Sur la base de près de 3 000 estimations de séroprévalence générées dans diverses enquêtes à ce jour7, probablement 35 à 55 % de la population mondiale avait été infectée au moins une fois à la fin 2021. À la fin 2021, probablement 73 à 81 % de la population mondiale avait été infectée. vaccinés, infectés ou les deux (Tableau 1). C’est peut-être même une sous-estimation. Ainsi, un seuil de 70 % pour la fin de la pandé‐ mie a déjà été franchi en 2021 et le SRAS-CoV-2 est entré dans sa phase endémique. Les poussées massives de variantes d’Omicron depuis fin 2021 ont ajouté beaucoup plus d’infections, mais se sont accompagnées d’une mortalité et d’un impact clinique plus faibles. 8 , 9 , 10 Bien qu’Omicron puisse également être intrinsèquement moins mortel, le tableau pourrait également s’expliquer en grande par‐ tie comme une variante d’évasion endémique surgissant contre l’immunité de base généralisée de la population.
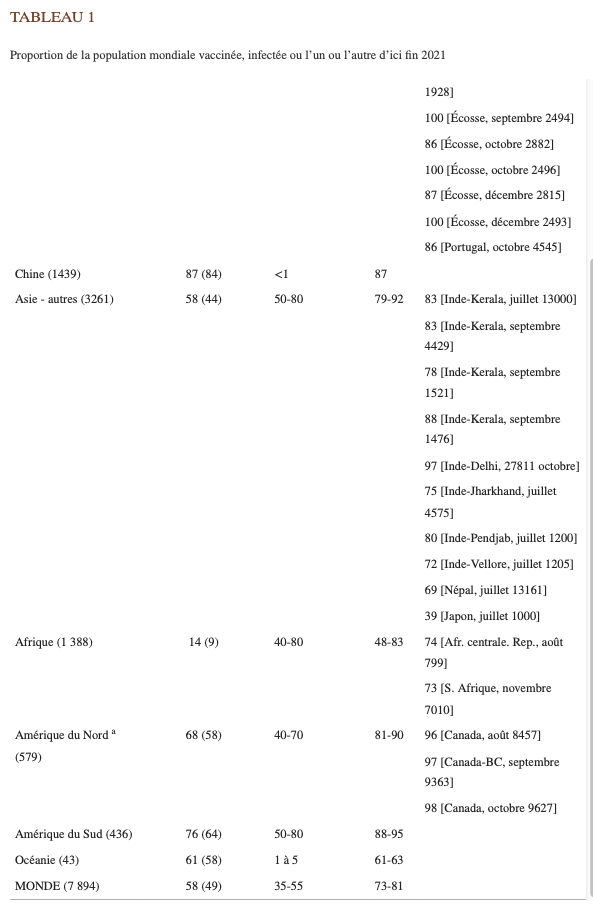
Note ajoutée au stade de la preuve
Depuis la dernière recherche, d’autres études ont été publiées qui montrent des niveaux de séroprévalence tout aussi élevés, voire plus élevés. Par exemple, selon les Centers for Disease Control and Prevention des États-Unis, les échan‐ tillons de sang des donneurs de sang aux États-Unis en décembre 2021 étaient positifs à 95 % pour les anticorps.
a Comprend l’Amérique centrale.
b Dans ce calcul, on suppose que la vaccination et l’infection naturelle sont indépendantes et que la proportion de personnes non vaccinées qui ont été infectées au moins une fois est la même que la proportion de personnes vaccinées qui ont été infectées au moins une fois. Cependant, en réalité, les personnes non vaccinées sont plus susceptibles d’avoir été infectées, parce que le vaccin offre une certaine protection contre l’infection et parce que les personnes vaccinées peuvent être plus soucieuses de leur santé que celles non vaccinées et sont donc moins susceptibles d’avoir été infectées. Par conséquent, la proportion de vaccinés ou d’infectés peut être plus importante que celle indiquée ici. À l’inverse, il peut être inférieur si les personnes vaccinées se livrent à des activités beaucoup plus non protégées qui compensent largement la protection offerte par la vaccination.
c Études sur des échantillons de ménages et de communautés, d’échantillons résiduels ou de donneurs de sang provenant de serotracker.com (recherche du 7 février 2022) incluant des adultes (avec ou sans enfants) avec une date de prélèvement intermédiaire après le 15 juillet 2021, évaluation des anticorps de pointe, > 100 échantillons évalués, aucun risque élevé de biais (tel qu’évalué par serotracker.com ). Le mois indiqué est le mois de la mi-date de prélèvement pour l’enquête de séroprévalence, mais le prélèvement peut s’être étendu sur plus d’un mois.
Les enquêtes de séroprévalence réalisées fin 2021 concordent avec ces estimations de l’immunité de la population (Tableau 1). 7 Il est vrai que les enquêtes peuvent être biaisées et seuls quelques pays dis‐ posent de données récentes. Cependant, presque tous les tableaux 1les données montrent des estima‐ tions de séroprévalence >70 % au second semestre 2021. Avec la poursuite des vaccinations et des in‐ fections, les estimations ont probablement encore augmenté depuis lors. Fin février 2022, 63 % de la population mondiale avait reçu un vaccin (55 % étaient « entièrement » vaccinés), presque autant de personnes avaient probablement été infectées au moins une fois et probablement près de 90 % de la po‐ pulation mondiale était vaccinée ou infectée à moins une fois.
Même si 70 à 90 % de la population mondiale bénéficie d’une certaine immunité, une hétérogénéité peut exister d’une région à l’autre. Fin 2021, l’immunité de la population était probablement encore in‐ férieure à 70 % en Océanie, et des incertitudes subsistent concernant l’Afrique. Certains pays pauvres avec de faibles taux de vaccination ont peut-être également été relativement épargnés par les vagues in‐ fectieuses. A l’inverse, les pays d’Europe épargnés par de fortes vagues épidémiques (par exemple la plupart des pays scandinaves) ont atteint des taux de vaccination très élevés. Une hétérogénéité substan‐ tielle peut encore exister entre et au sein des pays et des petites communautés. Des poches à faible im‐ munité peuvent persister pendant des années, permettant des épidémies locales et régionales d’intensité au moins modérée. Il est important de noter que la vaccination ou l’infection ne garantissent pas tou‐ jours des réponses immunitaires efficaces ; et la durabilité et l’adéquation pour prévenir l’apparition de nouveaux variants et prévenir des conséquences cliniques graves comportent une incertitude considé‐ rable. 10 , 11 L’immunité de la population pourrait continuer à se renouveler avec de nouvelles infec‐ tions et vaccinations. La nécessité de vaccinations répétées nécessite une étude impartiale. Tout cela fait partie intégrante de la phase endémique, et non plus d’une pandémie. La diminution de l’immunité, la diminution de l’efficacité des vaccins, l’émergence de nouveaux variants (plus ou moins pathogènes) en raison de l’évolution et du rôle des réservoirs animaux bien documentés pourraient façonner l’émer‐ gence et l’ampleur des vagues épidémiques du SRAS-CoV-2 à l’avenir et plusieurs d’entre elles. les fac‐ teurs sont imprévisibles. Pour un examen de l’immunité naturelle, vaccinale et hybride et de leurs taux de déclin, voir la réf. 12
3. BILAN DES MORTS
3.1. Nombre de morts « normal », COVID‐19 et pandémies passées
Il est important de comprendre à quel point cette pandémie nous a éloignés de la « normale », pour comprendre ce que signifierait un « retour à la normale ». « Normal » est déjà un concept insaisissable, car des fluctuations substantielles existent d’une année à l’autre et une grande variabilité (largement in‐ expliquée) existe chaque année dans différents pays et lieux. On peut comparer les récentes saisons ty‐ piques de grippe aux charges de mortalité respectives des pandémies passées des 20e et 21e siècles (Ta‐ bleau 2). Pour une comparaison équitable, il convient de tenir compte de la taille de la population mon‐ diale. De plus, il faut tenir compte de la répartition par âge des décès dus à une infection et de l’espé‐ rance de vie à ce moment-là pour estimer les années-personnes perdues parmi les personnes décédées. Enfin, on peut exprimer l’ampleur de la pandémie en proportion du nombre total d’années-personnes de vie attendues pour la population à cette époque qui ont été perdues à cause des décès dus à l’infec‐ tion. Par exemple, si une population a une espérance de vie cumulée de 100 000 années-personnes et que les décès dus à des infections génèrent 1 000 années-personnes perdues, la proportion perdue est de 1 %. En outre, l’ajustement de la qualité de vie en fonction des années-personnes perdues est utile, mais nécessite des données méticuleuses.
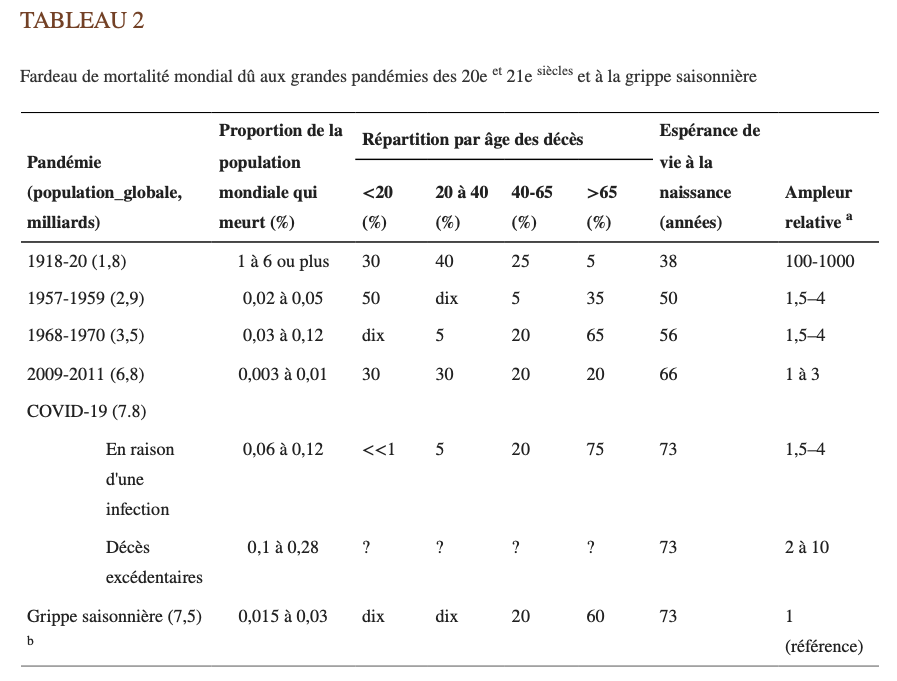
Note
Les estimations des décès et de leur répartition par âge comportent une très grande incertitude pour toutes les pandé‐ mies ainsi que pour la grippe saisonnière et une extrême prudence est de mise. Pour la grippe saisonnière, les calculs antérieurs se sont concentrés sur les données de surmortalité respiratoire, mais on estime que la mortalité toutes causes confondues due à la grippe pourrait être le double de ces chiffres. 22 , 23 Pour la pandémie de 2009, les calculs anté‐ rieurs se sont principalement concentrés sur 2009 et sur la mortalité respiratoire, mais des décès supplémentaires sont survenus plus tard en 2010 et 2011 et dans les pays durement touchés, il semble que la mortalité toutes causes confon‐ dues (y compris la mortalité cardiovasculaire) due à la grippe représentait le double de la mortalité respiratoire. 21 Pour les pandémies de 1957-1959 et de 1968-1970, les estimations sont basées sur des données de surmortalité respiratoire, mais cela peut également conduire à des sous-estimations. 17 , 18 , 19 L’incertitude est la plus élevée pour la grippe es‐ pagnole, où des estimations très différentes ont été proposées sur la base de données très fragmentaires. 13 , 14 , 15 , 16 Pour le COVID‐19, deux ensembles distincts sont fournis ici, un pour les décès dus à l’infection par le SRAS‐CoV‐2 et un autre pour les décès excédentaires toutes causes confondues. Bien que cette distinction ne soit peut-être pas aussi pertinente pour la grippe saisonnière et les pandémies antérieures des 100 dernières années, elle peut être extrêmement pertinente pour le COVID‐19, dans la mesure où des mesures beaucoup plus agressives ont été prises et où il y a eu de nombreux effets indirects de la pandémie et des mesures. pris sur divers aspects des soins de santé et de la santé (pro‐ bablement pour la plupart nocifs). Par exemple, alors que seulement << 1 % des décès dus à l’infection par le SRAS- CoV-2 sont survenus chez des enfants et des adolescents, l’excès de décès toutes causes confondues peut refléter une part plus importante de décès parmi ces populations jeunes dans les pays à revenu non élevé. en raison de la famine in‐ duite et d’autres difficultés, tandis que les enfants riches des pays à revenu élevé n’ont probablement pas connu de sur‐ mortalité à court terme et ont peut-être eu encore moins de décès dus à certaines causes (par exemple les accidents). Les proportions de décès dans chacune des quatre tranches d’âge présentées (<20, 20-40, 40-65, >65 ans) ne sont qu’approximatives et nécessitent une extrême prudence. Il est basé sur les réf. 13 , 14 , 15 , 16 , 17 , 18 , 19 , 20 , 21 , 22 , 23 et généralement, les informations stratifiées par âge ne sont disponibles que pour certains pays (et doivent être extrapolées à l’échelle mondiale) et/ou uniquement pour certains types de décès (par exemple, mortalité respiratoire).
Les écarts entre les différentes sources et calculs peuvent être importants et la répartition par âge des décès diffère se‐ lon les pays (par exemple, pour 1957 et 1968, l’âge moyen du décès en Europe et aux États-Unis est estimé à 65 et 62 ans, respectivement). Même pour la grippe saisonnière, la répartition par âge peut varier d’une saison à l’autre, par exemple Iuliano et al. 23 estiment entre 9 243 et 105 690 décès par an les enfants de moins de 5 ans, sur la base des données de 92 pays, et un total de 290 à 645 000 décès respiratoires dus à la grippe saisonnière. De plus, les estima‐ tions de l’ampleur relative se rapportent à la situation mondiale et à l’ensemble de la période d’intérêt. Les pics de sur‐ mortalité peuvent être bien plus extrêmes dans des lieux et des périodes spécifiques où il y a une forte activité épidé‐ mique et cela est vrai même pour la grippe saisonnière. Les différences entre les zones durement touchées et les zones épargnées chaque année sont généralement plus de 10 fois supérieures. Enfin, il existe une grande incertitude quant aux décès dus au COVID‐19, en particulier dans les pays à faible revenu, et une certaine incertitude existe même dans les pays à revenu élevé. Des séries d’autopsies dans les pays à revenu élevé 27 , 28 , 29 , 30 , 31 suggèrent que 55 à 95 % des décès déclarés dus au COVID-9 sont effectivement dus au COVID-19, mais le nombre d’autopsies est limité et elles sont très sélectionnées. À l’inverse, les décès dus au COVID‐19 ont dû être manqués, en particulier lors des pre‐ mières vagues en raison du nombre limité de tests. Les audits des certificats de décès et des dossiers médicaux de‐ vraient être effectués plus systématiquement. Certains comtés américains ont révisé à la baisse leur nombre de décès dus au COVID-19 32 , 33 et les données préliminaires de Gangelt en Allemagne 34 suggèrent également certains décès non liés au COVID-19 codés comme COVID-19. Dans les pays à revenus non élevés, les estimations spéculées sur les décès dus au COVID-19 varient considérablement. Les estimations utilisent généralement des calculs de surmortalité 35 , 36 , 37 qui reposent sur de nombreuses hypothèses et qui ne peuvent pas faire la différence entre les décès dus au COVID‐19, les décès indirectement induits par la pandémie et les décès induits par les mesures prises. Une dernière source d’incertitude est de savoir où mettre fin à la période pandémique et/ou s’il faut recourir à des fins asynchrones dans les différents pays.
a Basé sur la proportion d’années-personnes perdues.
b En comptant un total de 3 saisons, pour une comparaison équitable avec les cercles pandémiques.
Il existe une grande ambiguïté quant au nombre de décès causés par la grippe au cours de chaque pan‐ démie passée (tableau 2). Les décès estimés dus à la grippe espagnole varient de 17 à plus de 100 mil‐ lions, 13 , 14 , 15 , 16 , 17 , les chiffres typiques de la pandémie de 1957-1959 sont de 0,7 à 1,5 million, 18 la grippe de Hong Kong pourrait avoir causé 1 à 4 millions de décès. 19 et le nombre de décès liés à la pandémie de 2009 varient entre ~0,2 et ~0,6 million, mais ces estimations ne tiennent pas compte de certains décès supplémentaires survenus plus tard en 2010-2011. 20 , 21 Même les estimations des décès dus à la grippe saisonnière varient : 0,3 à 0,65 million de décès respiratoires par an sont estimés, mais la mortalité due à la grippe toutes causes confondues (y compris les décès cardiovasculaires) peut être le double de ces chiffres. 22 , 23 Quant au COVID‐19, malgré près d’un demi-million d’articles scienti‐ fiques rédigés en 2020-2021, 24 , 25 son nombre exact de décès reste débattu. Il y a probablement à la fois un sur- et un sous-dénombrement des décès dans différents contextes et sur la base de différentes définitions 26 ; et le nombre de décès dus à la pandémie dépend également du moment exact où se ter‐ mine la phase pandémique, passant à la phase endémique. Les efforts d’autopsie 27 , 28 , 29 , 30 , 31 et de vérification des certificats de décès ou des dossiers médicaux à ce jour 32 , 33 , 34 sont encore très frag‐ mentaires et préliminaires, et les évaluations des décès excessifs sont difficiles et montrent une grande variabilité. 35 , 36 , 37 Les comparaisons entre pandémies sont également précaires, car les pandémies passées nécessitaient des tests viraux limités, tandis que la COVID‐19 a inauguré des tests massifs.
En tenant compte de ces mises en garde, pour le COVID-19, 1957-9, 1968-70 et 2009-11, leur ampleur relative (en proportion des années-personnes perdues à cause de l’infection) était probablement de 1,5 à 4 fois l’ampleur « normale » de trois années consécutives. , années typiques de grippe saisonnière. Dans l’ensemble, la surmortalité pandémique et les décès dus à l’infection étaient probablement très proches
pour 1957-1959, 1968-1970 et 2009-11. À l’inverse, pour la pandémie de COVID‐19, les décès excé‐ dentaires peuvent être nettement supérieurs aux décès causés directement par le SRAS‐CoV‐2, et in‐ clure les décès causés par les perturbations induites à la fois par la pandémie et par les mesures agres‐ sives prises. La grippe espagnole présente la plus grande incertitude quant à son impact sur la mortali‐ té, mais elle se situe probablement dans une catégorie totalement différente. Cependant, une autre diffi‐ culté dans les comparaisons entre différentes pandémies s’étendant sur plus d’un siècle est que la dispo‐ nibilité des différentes options de gestion du traitement (par exemple, les soins intensifs) et l’accès des personnes à ces dernières ont beaucoup changé au fil du temps. De même, la disponibilité et le déploie‐ ment de vaccins efficaces ont beaucoup varié. De plus, les différentes mesures restrictives prises lors de différentes pandémies peuvent avoir entraîné différents avantages et inconvénients directs et indirects. Il n’entre pas dans le cadre de cet article de discuter des avantages et des inconvénients relatifs de diffé‐ rentes mesures non pharmacologiques. Il est possible que l’impact mortel relatif de la grippe espagnole aurait été moindre si le même virus avait frappé pour la première fois en 2019 plutôt qu’il y a un siècle.
3.2. Hétérogénéité
Les comparaisons au sein de pays et de lieux spécifiques peuvent montrer une ampleur relative diffé‐ rente de ces pandémies. Le COVID‐19 s’est distingué en affectant de manière disproportionnée les pays à revenu élevé (du moins en ce qui concerne les cas documentés et les décès), car ces pays comptent beaucoup plus de personnes âgées et des comorbidités plus fréquentes telles que l’obésité. Un sentiment accru de menace est apparu parce que le COVID‐19 a touché les épicentres de l’information et du pou‐ voir mondiaux. À l’inverse, alors que 800 millions de personnes dans le monde vivent dans la faim, 2 milliards supplémentaires vivent dans une faim cachée, et les décès dus à la faim (principalement des jeunes) sont bien plus nombreux que les décès dus au COVID-19 et augmentent rapidement avec la ré‐ ponse à la pandémie, les conflits et le changement climatique. 38 , 39 cette dévastation a reçu une atten‐ tion embarrassante et négligeable par rapport à la COVID‐19.
De plus, l’ampleur relative des pandémies varie considérablement selon les groupes d’âge. Le COVID‐ 19 a probablement causé beaucoup moins de décès chez les enfants et adolescents de moins de 20 ans (~ 20 000) 40 contre 3 saisons de grippe typique. 23 À l’inverse, la grande majorité des décès dus au COVID‐19 dans le monde sont survenus chez des personnes de plus de 65 ans, dont probablement en‐ viron 1 million de décès parmi les résidents institutionnalisés d’établissements de soins de longue du‐ rée. 41 , 42 Une grande partie des nouveaux décès excédentaires dans ces établissements étaient proba‐ blement dus à l’abandon, à la soif et à la faim. 42
3.3. Retour à la normale
Un « retour à la normale » n’est pas brutal et son rythme varie selon les pays et les populations. Une di‐ minution des décès dus au COVID‐19 (globalement et par groupe d’âge) pour revenir aux niveaux ty‐ piques de la grippe saisonnière ne se produira pas nécessairement en 2022 ou même au-delà. Avec une population mondiale de plus en plus vieillissante et des tests massifs, la « normale » peut encore corres‐ pondre à un nombre de décès plus élevé que les maladies liées à la grippe avant la COVID-19. Il ne faut pas considérer cela comme une phase pandémique continue. En outre, les pics saisonniers de décès pourraient se poursuivre, plus élevés dans certaines régions que dans d’autres. Bien que certaines zones soient davantage touchées chaque année pour des raisons mal comprises, les pics s’accompagnent souvent d’une faible immunité locale due à un déclin des réponses immunitaires et/ou à des variantes de fuite.
Fin 2021, seuls cinq pays comptant plus d’un million d’habitants avaient un taux de décès dus au CO‐ VID-19 sur 7 jours supérieur à 70 par million d’habitants. Tous ces pays se trouvaient en Europe de l’Est et avaient une faible couverture vaccinale (Géorgie 25 %, Hongrie 62 %, Pologne 53 %, Croatie 47 %, Bulgarie 30 % au 1er novembre 2021). 5 Il est important de noter que la couverture vaccinale était faible dans ces pays, en particulier pour les personnes âgées (qui contribuent à la plupart des décès). Sans surprise, fin février 2022, les taux de décès dus au COVID-19 par population les plus élevés étaient encore observés dans les pays d’Europe de l’Est et dans certains autres pays/localités comptant de nombreuses personnes âgées fragiles et/ou défavorisées, de faibles taux de vaccination des per‐ sonnes âgées et des systèmes de santé en difficulté à cause de l’austérité. (par exemple en Grèce) ou de fortes inégalités (par exemple aux États-Unis), mais même là, les tendances en matière de mortalité s’amélioraient. (Remarque ajoutée au stade de la preuve : fin mars 2022, aucun pays au monde n’avait de décès dus au COVID-19 sur 7 jours dépassant 45 par million d’habitants, à l’exception de Hong Kong qui menait depuis longtemps une politique zéro COVID et avait une couverture vaccinale sous- optimale parmi les personnes âgées. .)
4. CHARGE CLINIQUE
Les pandémies mettent à rude épreuve l’ensemble du système de santé. La discussion ici se concentre‐ ra, à titre d’illustration, sur les lits de soins intensifs, car la pression est perçue comme plus critique que pour les lits d’hôpitaux ordinaires (qui connaissent de toute façon des pics et des creux d’utilisation as‐ sez similaires). Cependant, la perturbation des soins primaires est également majeure et peut entraîner des conséquences majeures (par exemple, perturbation des services de prévention). 43
Dans 23 pays disposant de données (tableau 3), 44 , 45 , 46 La COVID‐19 a occupé plus de 25 % de la capacité en lits des soins intensifs prépandémiques pendant une moyenne de 2 mois de novembre 2020 à février 2021. La période moyenne d’occupation aussi élevée par la COVID‐19 était inférieure à la moitié au cours de la période respective de novembre 2021 à février 2022, même si tous ces pays ont connu un pic élevé (puis un recul) des ondes Omicrons au cours de cette période : 4 à 39 % de leur po‐ pulation avaient documenté une infection au cours de ces 4 mois (le nombre total d’infections peut être le double) ou plus). La plupart des pays (13 sur 23) n’ont connu aucune période entre novembre 2021 et février 2022 où l’occupation des lits liés au COVID‐19 représentait plus de 25 % de la capacité de leurs unités de soins intensifs avant la pandémie. Étant donné que de nombreux pays ont également augmen‐ té leur capacité en soins intensifs pendant la pandémie, la période pendant laquelle le stress a été élevé a probablement été encore plus courte. Dans les 10 pays où le taux d’occupation des lits liés au CO‐ VID‐19 dépassait 25 % de leur capacité d’accueil avant la pandémie, les pics ont été plus faibles au cours de la saison 2021-2022 qu’en 2020-2021.
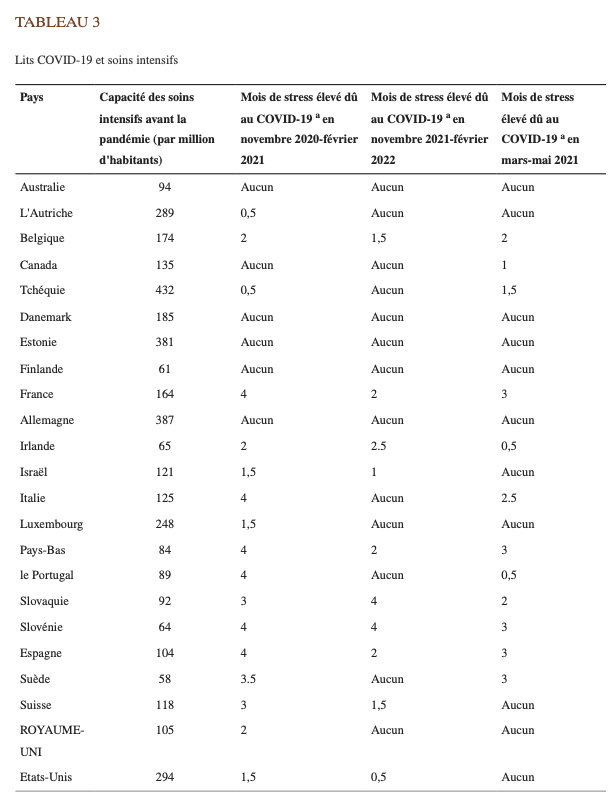
Note
La capacité en lits de soins intensifs avant la COVID-19 est obtenue à partir de la figure 5.18 sur https://www.oecd-ili‐ brary.org/sites/e5a80353-en/index.html?itemId=/content/component/e5a80353-en et https:/ /www.oecd.org/coronavi‐ rus/en/data‐insights/intensive-care-beds-capacity et également complété par Wikipédia ; lorsque différentes sources ont fourni des données, le plus grand nombre est affiché. Les données sur l’utilisation des lits de soins intensifs COVID‐19 proviennent de Notre monde en chiffres ( https://ourworldindata.org/covid‐hospitalizations ).
Abréviation : ND, aucune donnée.
(a) Nombre de mois avec des lits de soins intensifs COVID‐19 représentant au moins 25 % de la capacité totale en lits de soins intensifs prépandémiques ; administré en demi-mois environ, car le nombre de lits en soins intensifs avant la pandémie n’est pas standardisé d’un pays à l’autre ; en outre, de nombreux pays ont considérablement augmenté leur capacité en lits de soins intensifs pendant la pandémie.
Pour 12 des 23 pays, le taux d’occupation des lits en USI COVID‐19 dépassait également 25 % de leur capacité d’avant la pandémie au cours du printemps 2021. Au début du printemps 2022, seuls 2 de ces pays (Slovaquie et Slovénie) avaient un taux d’occupation COVID‐19. qui dépassait 25 % de leur capa‐ cité en lits de soins intensifs avant la pandémie.
5. RISQUE PERSONNEL RÉEL ET PERÇU
Les pandémies suscitent chez de nombreuses personnes une crainte justifiée pour leur vie. Le taux de létalité par infection (IFR, risque de mourir en cas d’infection) est essentiel pour la perception du risque. Le COVID‐19 présente un énorme gradient de risque lié à l’âge et le risque est également modi‐ fié par la présence de plusieurs comorbidités de la maladie. 47 Les premières estimations de l’IFR étaient exagérées. À l’échelle mondiale, jusqu’au début de 2021, l’IFR était probablement de 0,15 à 0,23 %, 48 , 49 bien que des estimations inférieures (0,11 %) 50 et supérieures 51 aient été proposées. Les différences concernent principalement le risque précis pour les personnes âgées, tandis que les analyses s’accordent sur le risque très faible des couches d’âge plus jeunes. 52 L’IFR était sensiblement différent selon les pays et les lieux, non seulement en raison de la structure d’âge différente, mais également en raison de taux très différents de comorbidités de fond, de succès différents dans la protection des popu‐ lations vulnérables (par exemple, les personnes institutionnalisées ou immunodéprimées), d’utilisation différente de médicaments efficaces ou inefficaces. /interventions néfastes et différents systèmes de san‐ té. Les estimations indicatives de l’IFR sont de 52 0,001 %, 0,01 %, 0,023 %, 0,05 %, 0,15 % et 0,49 %, de 0 à 19 ans, de 20 à 29 ans, de 30 à 39 ans, de 40 à 49 ans, de 50 à 59 ans et de 60 à 69 ans. , respecti‐ vement. En 2020, l’IFR était de 2,2 % chez les personnes âgées de plus de 70 ans vivant dans la com‐ munauté dans les pays à revenu élevé, probablement beaucoup plus faible chez les personnes âgées dans d’autres pays, et nettement plus élevé chez les résidents fragiles de soins de longue durée. 52
Avec l’avènement de la vaccination, l’IFR a probablement diminué considérablement. Si la vaccination maintient une efficacité de 80 % pour éviter la mort des personnes infectées (probablement une estima‐ tion prudente) 53 , 54 , 55 , les estimations IFR ci-dessus devraient être diminuées de 5 fois pour les per‐ sonnes vaccinées ; par exemple, pour les personnes âgées de plus de 70 ans vaccinées vivant dans la communauté, l’IFR peut avoir diminué à 0,45 % ; pour les 50-59 ans, ce serait 0,03 %. Pour les per‐ sonnes précédemment infectées, l’IFR est probablement également beaucoup plus faible que chez les personnes non infectées, bien qu’il soit difficile d’obtenir des chiffres exacts actuellement. Le maintien de chiffres IFR très bas dépendra de la persistance de la protection assurée par la vaccination ou les in‐ fections, y compris les événements répétés. L’amélioration des options de traitement devrait également se traduire par une réduction encore plus importante de l’IFR. 56 , 57 , 58
Des considérations similaires s’appliquent à d’autres conséquences graves, outre le décès. Ils ne s’ap‐ pliquent pas au risque d’infection, pour lequel une infection ou une vaccination antérieure semble conférer une protection bien moindre que dans le cas d’issues difficiles. 59 La compensation des risques (expositions accrues des personnes vaccinées) érode encore davantage la protection. 60 Par conséquent, si la perception du risque se concentre sur le nombre de cas documentés, la fausse perception des situa‐ tions d’urgence peut être difficile à réprimer.
Il est important de noter que le risque réel peut avoir moins d’importance que le risque perçu. De nom‐ breuses personnes ont des perceptions très déformées quant au risque de mauvais résultats après une in‐ fection par le SRAS‐CoV‐2. Par exemple, aux États-Unis, un tiers de la population estime que plus de la moitié des personnes infectées doivent être hospitalisées. 61 À l’inverse, le risque d’hospitalisation parmi les cas documentés était respectivement d’environ 7 % et 3 % lors des vagues Delta et Omicron. 62 Étant donné que les infections pourraient être 2 à 4 fois plus nombreuses que les infections documen‐ tées, le risque d’hospitalisation après une infection n’était probablement que de 1 à 2 %. En moyenne, la population américaine pensait également début 2021 que 8 % des décès étaient survenus chez des per‐ sonnes de moins de 24 ans61, alors que le pourcentage réel était d’environ 0,1 % à cette époque (0,3 % début 2022). Dans une autre enquête menée en Autriche, 63 enfants et adolescents pensaient qu’ils cou‐ raient un risque de 1,2 à 3,3 % d’être hospitalisés à cause du COVID‐19 en un an, soit plus de 1 000 fois plus élevé que la réalité, et ils avaient également une perception du risque massivement exagérée. pour leurs parents. Une autre difficulté dans l’appréciation du risque est que la probabilité d’une longue CO‐ VID et de séquelles à long terme de l’infection est encore estimée avec une grande incertitude. Il existe une grande hétérogénéité entre les groupes de population quant à l’ampleur de la perception exagérée des risques, et certaines personnes peuvent sous-estimer les risques par rapport à la réalité. La percep‐ tion du risque peut être importante pour façonner la réponse à la COVID‐19, aux comportements, à la dépression et à la santé mentale. 64 , 65 , 66 , 67 , 68 Un (re)calibrage approprié de la perception du risque est essentiel pour une véritable transition vers la phase endémique.
6. MESURES RESTRICTIVES
Au sens large, une pandémie peut persister quels que soient les indicateurs épidémiques et cliniques, si des mesures restrictives agressives continuent d’être en place et/ou si l’attention et la préoccupation à son égard restent accrues. L’indice de rigueur d’Oxford pour les mesures gouvernementales 69 , 70 était inférieur fin 2021 par rapport à un an plus tôt dans la plupart des pays, mais une grande partie de la po‐ pulation mondiale a continué de subir des mesures restrictives agressives et il en était de même fin fé‐ vrier 2022 (Figure 1). De plus, en 2021 et au début de 2022, de nombreux nouveaux types de mesures ont été adoptés, alors que les gouvernements et les autorités de santé publique ont affrété des territoires périlleux et se sont précipités pour mettre en place de nouvelles mesures. Les mandats et les mesures qui discriminent les personnes en fonction de leur statut lié à la pandémie (par exemple, le carnet de vaccination) peuvent être particulièrement problématiques. Il faut éviter de favoriser les divisions, la discorde et le recul des normes démocratiques. 71 , 72 , 73 , 74
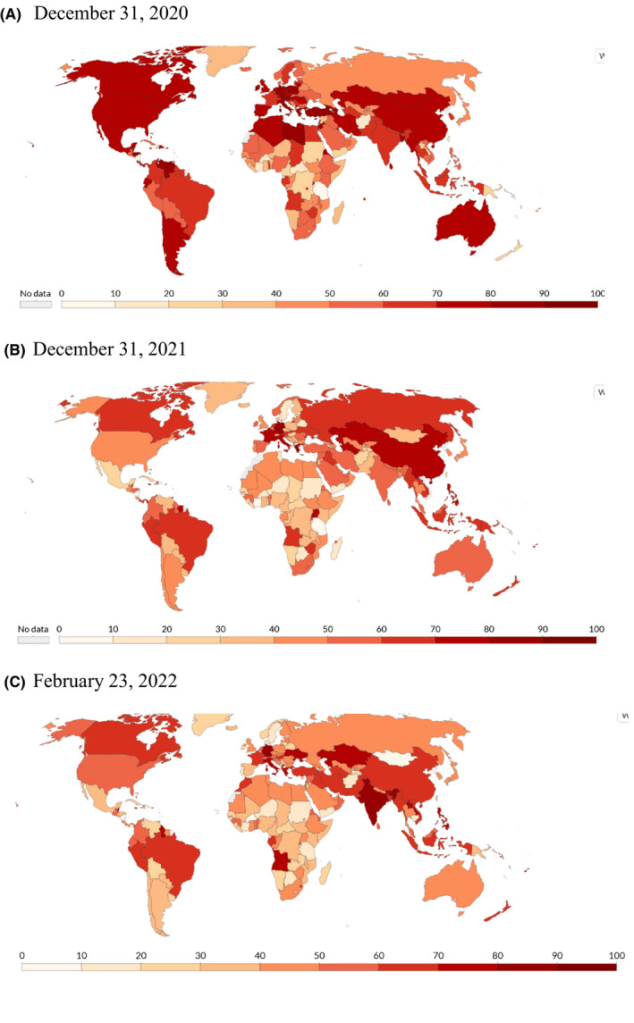
Indice de rigueur d’Oxford pour la réponse gouvernementale au COVID‐19. (A) 31 décembre 2020, (B) 31 décembre 2021, (C) 23 février 2022
7. ATTENTION DU PUBLIC REÇUE
7.1. Médias et réseaux sociaux
Le COVID‐19 a monopolisé l’attention du public à partir du début de l’année 2020. La couverture du COVID‐19 a représenté 25 % des 26 millions d’articles de presse publiés en première page de 172 prin‐ cipales sources d’information en ligne dans 11 pays entre janvier et octobre 2020.75 La présence sur les réseaux sociaux a également été très forte. Une base de données de tweets liés au COVID-19 compre‐ nait au 27 décembre 2021 un total de 2,17 milliards de tweets pertinents. 76 Les réseaux sociaux et les médias sont responsables d’une infodémie massive (une épidémie d’information qui comprend beaucoup de désinformation et de désinformation). 77 , 78 Un signe fort de la fin de la pandémie serait la ré‐ duction drastique de l’attention du public. 1 Cependant, les médias et les réseaux sociaux sont incités à maintenir une attention accrue longtemps après que les indicateurs épidémiologiques et cliniques soient entrés sur le territoire de l’endémicité. La polarisation et le triste enchevêtrement politique dans le contexte du COVID‐19 aggravent les perspectives.
7.2. Science
La science a également été radicalement affectée par la pandémie de COVID‐19, d’une manière sans précédent. 79 Plus de 400 000 articles liés au COVID‐19 ont été publiés en 2020-2021. 24 , 25 Dans Sco‐ pus (avec des données datant d’août 2021), 98 des 100 articles scientifiques les plus cités en 2020 étaient liés au COVID‐19 ; ce chiffre est tombé à 75/100 des articles les plus cités en 2021, mais il reste extraordinairement élevé. 80 Le fait que de nombreux scientifiques se soient mêlés à l’actualité, aux guerres sur les réseaux sociaux 81 et même aux agendas politiques et financiers liés au COVID‐19 ne présage rien de bon. Un intérêt scientifique exagéré pourrait prolonger les perceptions de la pandémie.
7.3. Santé publique
La santé publique a vaillamment combattu la COVID‐19. Que les résultats soient passables ou mé‐ diocres dans différents endroits, la rumination des échecs et une culture du blâme ne devraient pas pré‐ valoir. Nous pouvons décortiquer soigneusement ce que nous avons appris de cette expérience unique sans la perpétuer. Les autorités de santé publique devraient annoncer la fin de la pandémie. Cela ne si‐ gnifie pas que le problème est minimisé ou oublié de manière inappropriée, mais que nos communautés continuent de vivre. On ne sait pas quand la prochaine pandémie pourrait survenir : dans moins d’un an ou dans plus d’un siècle. Le SRAS-CoV-2 s’est avéré très imprévisible et l’imprévisibilité existe égale‐ ment pour la grippe. La préparation à une pandémie doit être soigneusement réfléchie et préorganisée 82 , mais ne doit pas perturber la vie.
8. HÉRITAGE PANDÉMIQUE
L’héritage de la pandémie comprend des effets sur d’autres dimensions de la santé (outre celles directe‐ ment dues au COVID‐19), sur la société, l’économie, la civilisation, la démocratie, les systèmes de va‐ leurs, etc. La pandémie et la réponse à celle-ci ont affecté la santé mentale 83 , 84 et physique, avec un excès de décès. 85 , 86 , 87 Le nombre total de décès excédentaires pourrait dépasser de loin ceux dus à l’infection par le SRAS-CoV-2. 35 , 36 Toutefois, les estimations de la surmortalité sont très prélimi‐ naires, elles dépendent de données faibles et d’hypothèses de modélisation fragiles et elles sont très in‐ certaines. Il est important de noter que la surmortalité comprend les effets indirects de la pandémie ain‐ si que les effets directs et indirects des mesures prises.
L’augmentation spectaculaire du nombre de personnes souffrant de la faim n’est qu’un aspect des dom‐ mages causés par les perturbations dues à la pandémie et aux mesures prises. Il existe encore une grande incertitude quant à l’impact relatif de la contraction économique et de l’inflation sur la santé. L’expérience passée des crises économiques montre un impact négatif majeur sur la santé, mais il n’existepasdeconsensustotaldanslalittérature88 ,89 ,90 ,91 ,92 ,93 ,94 ,95 ,96 ,97 ,98 ,99 ,100 ,101 et Le COVID‐19 est une situation très particulière. Le nombre de décès indirectement induits pourrait même dépasser celui du COVID‐19, mais cela dépendra en grande partie de la rapidité avec laquelle le choc économique pourra être inversé et de l’éventuelle survenue de complications supplémentaires (par exemple des guerres). Au moment d’écrire ces lignes, dans de nombreux pays, les taux d’inflation attei‐ gnaient déjà des valeurs supérieures à celles observées depuis des décennies, 102 , 103 , 104 par exemple 7,5 % aux États-Unis (données de janvier 2022), 5,6 % dans l’Union européenne (janvier 2022) et 5,9% en Nouvelle-Zélande (décembre 2021). L’augmentation des inégalités induite par la pandémie et les mesures prises aggrave la situation. La Banque mondiale prévoit que d’ici 2023, « toutes les économies avancées auront atteint une reprise complète de leur production ; Pourtant, la production dans les économies émergentes et en développement restera inférieure de 4 pour cent à sa tendance d’avant la pandémie. Pour de nombreuses économies vulnérables, le revers est encore plus important : la production des économies fragiles et touchées par un conflit sera inférieure de 7,5 pour cent à sa tendance d’avant la pandémie, et la production des petits États insulaires sera inférieure de 8,5 pour cent. 105 Les projec‐ tions doivent être considérées avec une extrême prudence, mais les personnes défavorisées et pauvres sont susceptibles de souffrir le plus, tant dans les pays pauvres que dans les pays à revenu élevé.
Des conséquences supplémentaires sur la santé peuvent apparaître à moyen ou long terme. 43 Leur im‐ pact exact dépend de la capacité à attirer l’attention sur ces problèmes au moins maintenant et à en atté‐ nuer l’impact. Continuer à ruminer les cas de COVID‐19 et d’autres indicateurs superflus du SRAS‐ CoV‐2 pourrait ne pas aider. L’impact à court, moyen et long terme sur la société, l’économie, la civili‐ sation, la démocratie et le système de valeurs fait l’objet de nombreux débats et sa discussion détaillée dépasse le cadre de cet article. Néanmoins, l’héritage de la pandémie pourrait continuer à nous hanter pendant des décennies, s’il entraîne des dommages irréversibles pour l’humanité à ces frontières.
LES RÉFÉRENCES
1. Robertson D, Doshi P. La fin de la pandémie ne sera pas télévisée . BMJ . 2021 ; 14 ( 375 ) :e068094. [ PubMed ] [ Google Scholar ]
2. Doshi P. La définition insaisissable de la grippe pandémique . Organisation mondiale de la santé Bull . 2011 ; 89 :532‐538. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
3. Dernier JM, éditeur. Un dictionnaire d’épidémiologie , 4e éd. Presse universitaire d’Oxford ; 2001. [ Google Scholar ]
4. Lavine JS, Bjornstad ON, Antia R. Les caractéristiques immunologiques régissent la transition du COVID‐19 vers l’endémicité. Sciences . 2021 ; 371 ( 6530 ):741‐745. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar
5. Notre monde dans les données . Vaccinations contre le coronavirus (COVID‐19) . https://ourworldindata.org/covid‐ vaccinations . Consulté le 24 février 2022
6. Bobrovitz N, Arora RK, Cao C et al. Séroprévalence mondiale des anticorps du SRAS‐CoV‐2 : une revue systématique et une méta‐analyse . PLoS Un . 2021 ; 16 ( 6 ): e0252617. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
7. Sérotracker. www.serotracker.com . Consulté le 24 février 2022
8. Équipe d’intervention COVID‐19 de l’Imperial College, Ferguson N, Ghni A, Hinsley W, Volz E. Rapport 50 : risque d’hospitalisation pour les cas d’Omicron en Angleterre . 22 décembre 2021. 10.25561/930352021. Consulté le 3 janvier 2022. [ CrossRef ]
9. Ulloa AC, Buchan SA, Daneman N, Brown KA. Estimations de la gravité de la variante Omicron du SRAS‐CoV‐2 en Ontario, Canada . JAMA . 2022 : e222274. est ce que je: 10.1001/jama.2022.2274. En ligne avant impression. [ Article gratuit PMC ] [ PubMed ] [ CrossRef ] [ Google Scholar ]
10. Lyngse FP, Mortensen LH, Denwood MJ et al. Transmission des COV du SRAS‐CoV‐2 Omicron dans les ménages danois . medRxiv . 2021. doi : 10.1101/2021.12.27.21268278 [ CrossRef ] [ Google Scholar ]
11. Goldberg Y, Mandel M, Bar-On YM et al. Déclin de l’immunité après le vaccin BNT162b2 en Israël . N Anglais J Med . 2021 ; 385 ( 24 ) : e85. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
12. Pilz S, Theiler‐Schwetz V, Trummer C, Krause R, Ioannidis JPA. Réinfections par le SRAS-CoV-2 : aperçu de l’efficacité et de la durée de l’immunité naturelle et hybride . Environ Rés . 2022 ; 209 : 112911. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
13. Murray CJL, Lopez AD, Chin B, Feehan D, Hill KH. Estimation de la mortalité potentielle due à une pandémie mondiale de grippe sur la base des données des registres d’état civil de la pandémie de 1918-1920 : une analyse quantitative . Lancette . 2006 ; 368 :2211‐2218. [ PubMed ] [ Google Scholar ]
14. Johnson NP, Mueller J. Mise à jour des comptes : mortalité mondiale de la pandémie de grippe « espagnole » de 1918-1920 . Taureau Hist Med . 2002 ; 76 : 105‐115. [ PubMed ] [ Google Scholar ]
15. Patterson KD, Pyle GF. La géographie et la mortalité de la pandémie de grippe de 1918 . Taureau Hist Med . 1991 ; 65 : 4‐ 21. [ PubMed ] [ Google Scholar ]
16. Spreeuwenberg P, Kroneman M, Paget J. Réévaluer le fardeau mondial de la mortalité de la pandémie de grippe de 1918″ . Am J Epidemiol . 2018 ; 187 ( 12 ):2561‐2567. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
17. Viboud C, Simonsen L, Fuentes R, Flores J, Miller MA, Chowell G. Impact mondial sur la mortalité de la pandémie de grippe de 1957 à 1959 . J Infecter Dis . 2016 ; 213 : 738‐745. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
18. Viboud C, Grais RF, Lafont BA, Miller MA, Simonsen L, Groupe d’étude multinational sur la mortalité saisonnière due à la grippe. Impact multinational de la pandémie de grippe de Hong Kong de 1968 : preuves d’une pandémie latente . J Infecter Dis . 2005 ; 192 ( 2 ):233‐248. [ PubMed ] [ Google Scholar ]
19. Honigsbaum M. Revisiter les pandémies de grippe de 1957 et 1968 . Lancette . 2020 ; 395 ( 10240 ):1824‐1826. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
20. Dawood FS, Iuliano AD, Reed C et al. Mortalité mondiale estimée associée aux 12 premiers mois de la circulation du virus de la grippe pandémique A H1N1 de 2009 : une étude de modélisation . Lancet InfectDis . 2012 ; 12 : 687‐695. [ PubMed
] [ Google Scholar ]
21. Simonsen L, Spreeuwenberg P, Lustig R et al. Estimations de la mortalité mondiale pour la pandémie de grippe de 2009 du projet GLaMOR : une étude de modélisation . Médecine PLoS . 2013 ; 10 :e1001558. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
22. Paget J, Spreeuwenberg P, Charu V et al. Mortalité mondiale associée aux épidémies de grippe saisonnière : nouvelles estimations de la charge et prédicteurs du projet GLaMOR . J Glob Santé . 2019 ; 9 ( 2 ):20421. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
23. Iuliano AD, Roguski KM, Chang HH et al. Estimations de la mortalité respiratoire associée à la grippe saisonnière à l’échelle mondiale : une étude de modélisation . Lancette . 2018 ; 391 ( 10127 ):1285‐1300. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
24. Organisation mondiale de la santé . Littérature mondiale COVID‐19 sur la base de données sur les maladies à coronavirus .https://search.bvsalud.org/global-literature-on-novel-coronavirus-2019-ncov/ . Consulté le 3 janvier 2022.
25. Ioannidis JPA, Salholz‐Hillel M, Boyack KW, Baas J. La croissance rapide et massive des auteurs du COVID‐19 dans la littérature scientifique . Royal Soc Open Sci . 2021 ; 8 :8210389210389. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
26. Ioannidis, juge de paix. Surestimation et sous-estimation des décès dus au COVID‐19 . Eur J Epidémiol . 2021 ; 36 ( 6 ): 581‐588. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
27. Romanova ES, Vasilyev VV, Startseva G, Karev V, Rybakova MG, Platonov PG. Cause de décès basée sur des études post‐ mortem systématiques chez des patients avec une PCR tissulaire positive au SRAS‐CoV‐2 pendant la pandémie de COVID‐19 . J Interne Med . 2021 ; 290 ( 3 ): 655‐665. doi: 10.1111/joim.13300 [ Article gratuit PMC ] [ PubMed ] [ CrossRef
] [ Google Scholar ]
28. Edler C, Schröder AS, Aepfelbacher M et al. Mourir avec une infection par le SRAS-CoV-2 – une étude d’autopsie des 80 premiers cas consécutifs à Hambourg, en Allemagne . Int J Legal Med . 2020 ; 134 ( 4 ): 1275‐1284. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
29. Elezkurtaj S, Greuel S, Ihlow J et al. Causes de décès et comorbidités chez les patients hospitalisés atteints de COVID‐19 . Représentant scientifique . 2021 ; 11 ( 1 ):4263. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
30. Danics K, Pesti A, Törő K et al. Une catégorisation des causes de décès, dépendante de l’association COVID-19, dans 100 cas d’autopsie . Géroscience . 2021 ; 43 ( 5 ):2265‐2287. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
31. De‐Giorgio F, Grassi VM, Bergamin E et al. Mourir, « de » ou « avec » la COVID‐19 pendant la pandémie : enjeux médico- légaux selon une perspective populationnelle . Int J Environ Res Santé Publique . 2021 ; 18 ( 16 ):8851. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
32. Actualités, A . « Le comté d’Alameda révise le nombre de décès dus au COVID-19 de 25 % » . https://abc7news.com/covid- death-count-alameda-county-deaths-19-cases/10755419/ . Consulté le 24 février 2022
33. Le nombre de décès dus au COVID-19 dans le comté de Bayarea N. Santa Clara diminue de 505 après la modification des données . https://www.nbcbayarea.com/news/local/santa-clara-countys-covid-19-death-toll-drops-by-505-after-data- change/2585739/ . Consulté le 24 février 2022.
34. Richter E, Liebl D, Schulte B et al. Analyse de l’impact des décès et des enquêtes de séroprévalence dans une communauté subissant un événement de propagation du SRAS-CoV-2 . medRxiv . 2022. est ce que je : 10.1101/2022.01.26.22269805 [ CrossRef ] [ Google Scholar ]
35. Karlinsky A, Kobak D. Suivi de la surmortalité dans les pays pendant la pandémie de COVID‐19 avec l’ensemble de données sur la mortalité mondiale . Élife . 2021 ; 10 :e69336. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
36. Adam D. Le véritable bilan de la pandémie : des millions de plus que les chiffres officiels . Nature . 2022 ; 601 ( 7893 ) : 312‐ 315. [ PubMed ] [ Google Scholar ]
37. Jha P, Deshmukh Y, Tumbe C et al. Mortalité due au COVID en Inde : données d’enquête nationale et décès dans les établissements de santé . Sciences . 2022 ; 375 ( 6581 ) :667‐671. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
38. Godecke T, Stein AJ, Qaim M. Le fardeau mondial de la faim chronique et cachée : tendances et déterminants . Glob Food Sécur . 2018 ; 17 :21‐29. [ Google Scholar ]
39. Oxfam. Le virus de la faim se multiplie . https://oi‐files‐d8‐prod.s3.eu‐west‐2.amazonaws.com/s3fs‐public/2021‐ 07/The%20Hunger%20Virus%202.0_media%20brief_EN.pdf (9 juillet 2021) . Consulté le 3 janvier 2022.
40. Mortalité infantile et COVID‐19 . https://data.unicef.org/topic/child‐survival/covid‐19 . Consulté le 3 janvier 2022.
41. Comas‐Herrera A, Zalakaín J, Lemmon E et al. Mortalité associée au COVID‐19 dans les maisons de retraite : données probantes internationales . Article dans LTCcovid.org, International Long‐Term Care Policy Network, CPEC‐LSE, 1er février 2021.
42. Heneghan C, Dietrich M, Brassey J, Jefferson T. Effets du COVID‐19 dans les maisons de retraite – Une revue de méthodes mixtes . Garantie mondiale. https://collateralglobal.org/article/effects-of-covid-19-in-care-homes/ . Consulté le 3 janvier 2022.
43. Ioannidis JPA. Perspective mondiale de l’épidémiologie du COVID‐19 pour une pandémie à cycle complet . Eur J Clin Invest . 2020 ; 7 :e13423. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
44. Capacité en lits de soins intensifs en 2020 ou année la plus proche . https://www.oecd.org/coronavirus/en/data‐ insights/intensive-care-beds-capacity . Consulté le 3 janvier 2022.
45. https://read.oecd‐ilibrary.org/view/?ref=119_119689‐ ud5comtf84&title=Beyond_Containment:Health_systems_responses_to_COVID‐19_in_the_OECD . Consulté le 3 janvier 2022.
46.Rhodes A, Ferdinande P, Flaatten H, Guidet B, Metnitz PG, Moreno RP. La variabilité du nombre de lits de soins intensifs en Europe . Soins intensifs Med . 2012 ; 38 : 1647‐1653. [ PubMed ] [ Google Scholar ]
47. Williamson EJ, Walker AJ, Bhaskaran K et al. Facteurs associés aux décès liés au COVID‐19 avec OpenSAFELY . Nature . 2020 ; 584 ( 7821 ) :430‐436. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
48. Ioannidis JPA. Taux de mortalité par infection au COVID‐19 déduit des données de séroprévalence . Bull Organe mondial de la santé . 2021 ; 99 ( 1 ):19‐33F. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
49. Ioannidis JPA. Réconcilier les estimations des taux mondiaux de propagation et de mortalité par infection du COVID‐19 : un aperçu des évaluations systématiques . Eur J Clin Invest . 2021 ; 51 ( 5 ): e13554. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
50. Ayoub HH, Mumtaz GR, Seedat S, Makhoul M, Chemaitelly H, Abu‐Raddad LJ. Estimations de l’exposition mondiale à l’infection par le SRAS‐CoV‐2, de la morbidité infectieuse et des taux de mortalité par infection en 2020 . Glob Epidémiol . 2021 ; 3 : 100068‐. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
51. O’Driscoll M, Dos Santos GR, Wang L et al. Modèles de mortalité et d’immunité par âge du SRAS-CoV-2 . Nature . 2021 ; 590 ( 7844 ) : 140‐145. est ce que je: 10.1038/s41586-020-2918-0 [ PubMed ] [ CrossRef ] [ Google Scholar
]
52. Axfors C, Ioannidis JPA. Taux de mortalité par infection au COVID‐19 dans les populations âgées vivant dans la
communauté . Eur J Epidémiol . 2022 ; 1‐15. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
53. Arbel R, Hammerman A, Sergienko R et al. Rappel du vaccin BNT162b2 et mortalité due au covid‐19 . N Anglais J Med . 2021 ; 385 ( 26 ) :2413‐2420. doi: 10.1056/NEJMoa2115624 [ Article gratuit PMC ] [ PubMed ] [ CrossRef
] [ Google Scholar ]
54. Bar-On YM, Goldberg Y, Mandel M et al. Protection contre le Covid‐19 par le rappel BNT162b2 dans toutes les tranches d’âge . N Anglais J Med . 2021 ; 385 ( 26 ) :2421‐2430. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
55. Ioannidis JPA. Estimation de l’efficacité conditionnelle du vaccin . SSRN Électron J. 2022. https://ssrn.com/abstract=4033819 %5B Google Scholar ]
56. Groupe collaboratif RECOVERY . Tocilizumab chez les patients admis à l’hôpital avec COVID‐19 (RECOVERY) : un essai sur plateforme randomisé, contrôlé et ouvert . Lancette . 2021 ; 397 ( 10285 ):1637‐1645. doi: 10.1016/S0140-6736(21)00676-0
[ Article gratuit PMC ] [ PubMed ] [ CrossRef ] [ Google Scholar ]
57. Groupe collaboratif RECOVERY, Horby P, Lim WS, Emberson JR, et al. Dexaméthasone chez les patients hospitalisés atteints de covid‐19 . N Anglais J Med . 2021 ; 384 ( 8 ): 693‐704. doi: 10.1056/NEJMoa2021436 [ Article gratuit PMC ] [ PubMed ] [ CrossRef ] [ Google Scholar ]
58. Pessoa-Amorim G, Campbell M, Fletcher L et al. Intégrer les essais aux bons soins cliniques : leçons de l’essai RECOVERY . Santé future J . 2021 ; 8 ( 2 ):e243‐e250. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
59. Katikireddi SV, Cerqueira‐Silva T, Vasileiou E, et al. Protection du vaccin ChAdOx1 nCoV‐19 à deux doses contre les hospitalisations et les décès liés au COVID‐19 au fil du temps : une étude de cohorte rétrospective basée sur la population en Écosse et au Brésil . Lancette . 2022 ; 399 ( 10319 ) :25‐35. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
60. Ioannidis JPA. Bénéfice de la vaccination contre la COVID‐19 en termes de compensation des risques potentiels . Vaccins Npj . 2021 ; 6 :99. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
61. https://www.brookings.edu/research/how‐misinformation-is-distorting-covid-policies-and-behaviors/ . Consulté le 3 janvier 2022.
62. Centres de contrôle et de prévention des maladies . www.cdc.gov . Consulté le 24 février 2022.
63. Schabus M, Eigl ES. «Maintenant, c’est à votre tour de prendre la parole!»‐Fardeaux et conséquences psychosociales de la
pandémie de COVID‐19 pour les enfants et adolescents autrichiens . 2021, osf.io.
64. Yıldırım M, Geçer E, Akgül Ö. Les impacts de la vulnérabilité, du risque perçu et de la peur sur les comportements préventifs
contre le COVID‐19 . Médecine de santé psychologique . 2021 ; 26 ( 1 ):35‐43. [ PubMed ] [ Google Scholar ]
65. Wong CML, Jensen O. Le paradoxe de la confiance : risque perçu et conformité du public pendant la pandémie de COVID‐19
à Singapour . J Risque Rés . 2020 ; 23 :1021‐1030. [ Google Scholar ]
66. Yıldırım M, Güler A. Analyse factorielle de l’échelle de risque perçu COVID‐19 : une étude préliminaire . Goujon de la mort
. 2020 ; 25 : 1‐8. [ PubMed ] [ Google Scholar ]
67. Marinthe G, Brown G, Delouves S, et al. Prendre soin de moi : explorer la relation entre la mentalité de complot, le risque personnel perçu et les mesures de prévention du COVID‐19 . Br J Psychol de la Santé . 2020 ; 25 : 957‐980. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
68. Kim AW, Nyengerai T, Mendenhall E. Évaluation des impacts sur la santé mentale de la pandémie de COVID-19 : le risque perçu d’infection par le COVID-19 et les traumatismes de l’enfance prédisent les symptômes dépressifs des adultes dans les zones urbaines d’Afrique du Sud . Psychol Med . 2020 ; 8 : 1‐13. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
69. Hallas L, Kira B, Luciano M et al. Variation dans les réponses gouvernementales au COVID‐19 »Version 12.0. Document de travail de l’École de gouvernement Blavatnik . www.bsg.ox.ac.uk/covidtracker . Consulté le 11 juin 2021.
70. https://www.bsg.ox.ac.uk/research/research-projects/covid-19-government-response-tracker . Consulté le 3 janvier 2022. 71. Schippers M, Ioannidis JPA. Sauver la démocratie de la pandémie . Tablette . 2022.
https://www.tabletmag.com/sections/science/articles/ savingdemocracyfrompandemic [ Google Scholar ]
72. Ioannidis JPA. Maladie à coronavirus 2019 : les méfaits des informations exagérées et des mesures non fondées sur des preuves . Eur J Clin Invest . 2020 ; 50 ( 4 ): e13222. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
73. Lewkowicz J, Woźniak M, Wrzesiński M. COVID‐19 et érosion de la démocratie . Modèle économique . 2022 ; 106 : 105682. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
74. Edgell AB, Lachapelle J, Lührmann A, Maerz SF. « Recul de la pandémie : violations des normes démocratiques pendant le Covid‐19 « . Soc Sci Med . 2021 ; 285 : 114244. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
75. Krawczyk K, Chelkowski T, Mishra S et al. Quantifier la couverture médiatique en ligne de la pandémie de COVID‐19 . J Med Internet Res . 2021 ; 23 :e28253. doi: 10.2196/28253 [ Article gratuit PMC ] [ PubMed ] [ CrossRef ] [ Google Scholar ]
76. Chen E, Lerman K, Ferrara E. Suivi du discours sur les réseaux sociaux sur la pandémie de COVID‐19 : développement d’un ensemble de données Twitter public sur les coronavirus . Enquête de santé publique JMIR . 2020 ; 6 ( 2 ): e19273. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
77. Kouzy R, Jaoude JA, Kraitem A, et al. Le coronavirus devient viral : quantifier l’épidémie de désinformation sur le COVID‐ 19 sur Twitter . Curéus . 2020 ; 12 :e7255. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
78. Zarocostas J. Comment lutter contre une infodémie . Lancette . 2020 ; 395 ( 10225 ):676. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
79. JPA Ioannidis. Comment la pandémie change les normes de la science . Tablette . 2021.https://www.tabletmag.com/sections/science/articles/pandemic‐science %5B Google Scholar ]
80. Ioannidis JPA, Bendavid E, Salholz‐Hillel M, Boyack KW, Baas J. Covidisation massive des citations de recherche et de l’élite des citations . medRxiv . 2022. est ce que je : 10.1101/2022.01.24.22269775 [ CrossRef ] [ Google Scholar
]
81. Ioannidis JP, Tezel A, Jagsi R. Impact global et spécifique des citations sur le COVID-19 d’experts médiatiques très visibles sur le COVID-19 : analyse bibliométrique . BMJ Ouvert . 2021 ; 11 ( 10 ):e052856. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
82. Maxmen A. La COVID nous a-t-elle appris quelque chose sur la préparation à une pandémie ? Nature . 2021 ; 596 ( 7872 ) : 332‐335. [ PubMed ] [ Google Scholar ]
83. Necho M, Tsehay M, Birkie M, Biset G, Tadesse E. Prévalence de l’anxiété, de la dépression et de la détresse psychologique au sein de la population générale pendant la pandémie de COVID‐19 : une revue systématique et une méta‐analyse . Int J Soc Psychiatrie . 2021 ; 67 ( 7 ):892‐906. [ PubMed ] [ Google Scholar ]
84. Collaborateurs en matière de troubles mentaux liés à la COVID‐19 . Prévalence mondiale et fardeau des troubles dépressifs et anxieux dans 204 pays et territoires en 2020 en raison de la pandémie de COVID‐19 . Lancette . 2021 ; 398 ( 10312 ):1700‐1712. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
85. Böttcher L, D’Orsogna MR, Chou T. Utilisation des décès excessifs et des statistiques de tests pour déterminer les mortalités liées au COVID‐19 . Eur J Epidémiol . 2021 ; 36 ( 5 ):545‐558. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
86. Islam N, Shkolnikov VM, Acosta RJ, et al. Surmortalité associée à la pandémie de covid‐19 en 2020 : analyse de séries chronologiques désagrégées par âge et sexe dans 29 pays à revenu élevé . BMJ . 2021 ; 373 : n1137. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
87. Woolf SH, Chapman DA, Sabo RT, Zimmerman EB. Excédent de décès dus au COVID‐19 et à d’autres causes aux États- Unis, du 1er mars 2020 au 2 janvier 2021 . JAMA . 2021 ; 325 ( 17 ): 1786‐1789. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
88. Baird S, Friedman J, Schady N. Chocs de revenus globaux et mortalité infantile dans le monde en développement . Rev Econ Stat . 2011 ; 93 ( 3 ):847‐856. [ Google Scholar ]
89. Burgard SA, Ailshire JA, Kalousova L. La grande récession et la santé : personnes, populations et disparités . Annales Am Acad Polit Social Sci . 2013 ; 650 ( 1 ):194‐213. [ Google Scholar ]
90. Cutler D, Deaton A, Lleras‐Muney A. Les déterminants de la mortalité . J Econ Persp . 2006 ; 20 ( 3 ):97‐120. [ Google Scholar ]
91. Gerdtham UG, Ruhm CJ. Les décès augmentent en période de conjoncture économique favorable : données probantes de l’OCDE . Eco Biol humain . 2006 ; 4 ( 3 ):298‐316. [ PubMed ] [ Google Scholar ]
92. Lin S-J. Fluctuations économiques et résultats en matière de santé : une analyse par panel des pays d’Asie‐Pacifique . Économie appliquée . 2009 ; 41 ( 4 ): 519‐530. [ Google Scholar ]
93. Maruthappu M, Watson R, Watkins J, Zeltner T, Raine R, Atun R. Effets des ralentissements économiques sur la mortalité infantile : une analyse économique mondiale, 1981-2010 . Santé mondiale du BMJ . 2017 ; 2 :e000157. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
94. Le juge en chef Ruhm. Les récessions sont-elles bonnes pour la santé ? QJ Économie . 2000 ; 115 ( 2 ): 617‐650. [ Google Scholar ]
95. Schady N, Smitz MF. Chocs économiques globaux et mortalité infantile : nouvelles données probantes pour les pays à revenu intermédiaire . Lettres économiques . 2010 ; 108 ( 2 ): 145‐148. [ Google Scholar ]
96. Tapia Granados JA, Ionides EL. Santé de la population et économie : mortalité et grande récession en Europe . Économie de la santé . 2017 ; 26 ( 12 ):219‐235. [ PubMed ] [ Google Scholar ]
97. Parmar D, Stavropoulou C, Ioannidis JP. Résultats en matière de santé pendant la crise financière de 2008 en Europe : revue systématique de la littérature . BMJ . 2016 ; 6 ( 354 ) :i4588. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
98. Stuckler D, Basu S, Suhrcke M, Coutts A, McKee M. L’effet sur la santé publique des crises économiques et les réponses politiques alternatives en Europe : une analyse empirique . Lancette . 2009 ; 374 : 315‐323. [ PubMed ] [ Google Scholar ]
99. Kentikelenis A, Karanikolos M, Papanicolas I, Basu S, McKee M, Stuckler D. Effets sur la santé de la crise financière : présages d’une tragédie grecque . Lancette . 2011 ; 378 : 1457‐1458. [ PubMed ] [ Google Scholar ]
100. Tapia Granados JA, Diez Roux AV. La vie et la mort pendant la Grande Dépression . Proc Natl Acad Sci USA . 2009 ; 106 :17290‐17295. [ Article gratuit PMC ] [ PubMed ] [ Google Scholar ]
101. Brainerd E, Cutler DM. Autopsie d’un empire : comprendre la mortalité en Russie et dans l’ex-Union soviétique . J Perspective économique . 2005 ; 19 : 107‐130. doi: 10.1257/0895330053147921 [ CrossRef ] [ Google Scholar
]
102. https://tradingnomics.com/united-states/inflation-cpi . Consulté le 24 février 2022.
103. https://ec.europa.eu/eurostat/documents/2995521/14245727/2‐23022022‐AP‐EN.pdf/1bd1f78c‐b615‐7052‐7379‐ 3129551900eb . Consulté le 24 février 2022.
104. https://www.rbnz.govt.nz/monetary‐policy/inflation . Consulté le 24 février 2022.
105. https://www.worldbank.org/en/news/press‐release/2022/01/11/global-recovery-economys-debt-commodity-inequality .
Consulté le 24 février 2022.