Publié le 05/02/2021
Covid-19 : utiliser l’azithromycine pour ce qu’elle est…

Chez les patients atteints d’une forme sévère de Covid-19, la réponse immunitaire de l’hôte joue un rôle clé dans le déclenchement de la pneumopathie aiguë. Les effets positifs des corticoïdes chez ces patients suggèrent que d’autres molécules ayant un effet immunosuppresseur ou immunomodulateur pourraient aussi améliorer le pronostic de ces patients.
Les macrolides, particulièrement l’azithromycine, possèdent cette activité immunomodulatrice. Ils réduisent la production de cytokines pro-inflammatoires et inhibent l’activation des neutrophiles. Ils sont largement utilisés pour leurs propriétés anti-bactériennes dans les pneumopathies et pour leurs effets immunomodulateurs dans les pathologies pulmonaires chroniques. L’azithromycine a montré sa capacité à inhiber in vitro la réplication du SARS-CoV-2 dans des cellules Véro et dans les cellules épithéliales humaines, à des concentrations obtenues par une posologie de 500 mg par jour.
Les résultats publiés jusqu’à présent ne permettent pas de conclure à l’efficacité des bénéfices cliniques des macrolides dans la prise en charge des patients atteints de Covid-19.
Malgré l’absence de recommandations, l’azithromycine a été largement utilisée, notamment en association avec l’hydroxychloroquine.
Le retour de RECOVERY
Le Lancet publie de nouvelles données, issus de l’étude RECOVERY menée au Royaume-Uni, qui testait l’efficacité de plusieurs molécules, dont l’azithromycine, sur les patients hospitalisés pour une Covid-19. Au total 7 763 patients ont été inclus (65 ans d’âge moyen, 1/3 de femmes). Les uns (n = 2582) recevaient 500 mg d’azithromycine par jour, en plus des soins habituels, les autres (n = 5 181) bénéficiaient des seuls soins habituels.
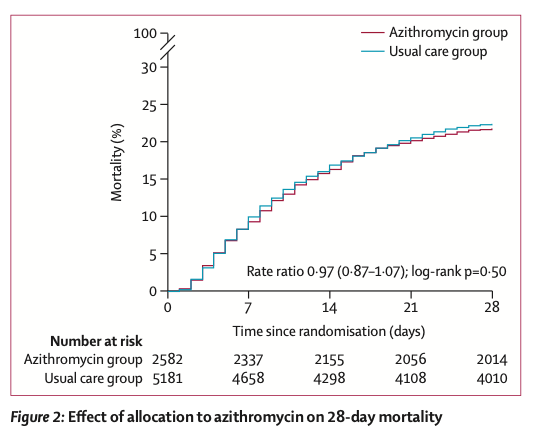
Les résultats de cette étude ne sont pas plus convaincants en termes d’efficacité, sur la mortalité (Risk Ratio RR 0,97 ; intervalle de confiance à 95 % IC : 0,87 à 1,07), la durée d’hospitalisation (10 jours vs 11 jours), ou la sortie d’hospitalisation dans les 28 jours (RR 1,04 ; IC : 0,98 à 1,10). Le bénéfice n’est pas prouvé non plus pour les patients ne nécessitant pas d’assistance ventilatoire à leur inclusion, sur le critère associant la nécessité de ventilation et le décès (RR 0,95 ; IC : 0,87 à 1,03).
Les auteurs précisent que les résultats sont solides et se maintiennent dans l’analyse en différents sous-groupes (âge, genre, origine, durée des symptômes, niveau de l’assistance respiratoire, utilisation de corticoïdes). Ils estiment que l’azithromycine devrait être réservée aux patients hospitalisés chez lesquels existe une réelle indication anti-bactérienne.
Dr Roseline Péluchon
RÉFÉRENCE
Groupe RECOVERY : Azithromycin in patients admitted to hospital with COVID-19 (RECOVERY): a randomised, controlled, open-label, platform trial. Lancet, 2021 ; publication avancée en ligne le 2 février. doi.org/10.1016/S0140-6736(21)00149-5
Azithromycin in patients admitted to hospital with COVID-19 (RECOVERY): a randomised, controlled, open-label, platform trial
- RECOVERY Collaborative Group †
- Show footnotesOpen AccessPublished:February 02, 2021DOI:https://doi.org/10.1016/S0140-6736(21)00149-5
https://www.thelancet.com/action/showPdf?pii=S0140-6736%2821%2900149-5
Background
Azithromycin has been proposed as a treatment for COVID-19 on the basis of its immunomodulatory actions. We aimed to evaluate the safety and efficacy of azithromycin in patients admitted to hospital with COVID-19.
Methods
In this randomised, controlled, open-label, adaptive platform trial (Randomised Evaluation of COVID-19 Therapy [RECOVERY]), several possible treatments were compared with usual care in patients admitted to hospital with COVID-19 in the UK. The trial is underway at 176 hospitals in the UK. Eligible and consenting patients were randomly allocated to either usual standard of care alone or usual standard of care plus azithromycin 500 mg once per day by mouth or intravenously for 10 days or until discharge (or allocation to one of the other RECOVERY treatment groups). Patients were assigned via web-based simple (unstratified) randomisation with allocation concealment and were twice as likely to be randomly assigned to usual care than to any of the active treatment groups. Participants and local study staff were not masked to the allocated treatment, but all others involved in the trial were masked to the outcome data during the trial. The primary outcome was 28-day all-cause mortality, assessed in the intention-to-treat population. The trial is registered with ISRCTN, 50189673, and ClinicalTrials.gov, NCT04381936.
Findings
Between April 7 and Nov 27, 2020, of 16 442 patients enrolled in the RECOVERY trial, 9433 (57%) were eligible and 7763 were included in the assessment of azithromycin. The mean age of these study participants was 65·3 years (SD 15·7) and approximately a third were women (2944 [38%] of 7763). 2582 patients were randomly allocated to receive azithromycin and 5181 patients were randomly allocated to usual care alone. Overall, 561 (22%) patients allocated to azithromycin and 1162 (22%) patients allocated to usual care died within 28 days (rate ratio 0·97, 95% CI 0·87–1·07; p=0·50). No significant difference was seen in duration of hospital stay (median 10 days [IQR 5 to >28] vs 11 days [5 to >28]) or the proportion of patients discharged from hospital alive within 28 days (rate ratio 1·04, 95% CI 0·98–1·10; p=0·19). Among those not on invasive mechanical ventilation at baseline, no significant difference was seen in the proportion meeting the composite endpoint of invasive mechanical ventilation or death (risk ratio 0·95, 95% CI 0·87–1·03; p=0·24).
Interpretation
In patients admitted to hospital with COVID-19, azithromycin did not improve survival or other prespecified clinical outcomes. Azithromycin use in patients admitted to hospital with COVID-19 should be restricted to patients in whom there is a clear antimicrobial indication.
Funding
UK Research and Innovation (Medical Research Council) and National Institute of Health Research.